分析化学
教你的学生解决所有行业的复杂问题
我们的集成解决方案帮助学生收集准确的数据,可视化趋势和关系,并为传统和创新实验探索不同的假设。
质量
多年来,学院和大学一直依靠我们的耐用硬件来帮助教师教授关键概念。
负担得起的
我们的技术是为学生设计和定价的。
多才多艺的
分析化学产品类别
示例数据

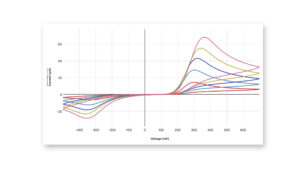
使用Go Direct研究不同浓度对乙酰氨基酚的循环伏安图®循环伏安法系统和游标仪器分析™
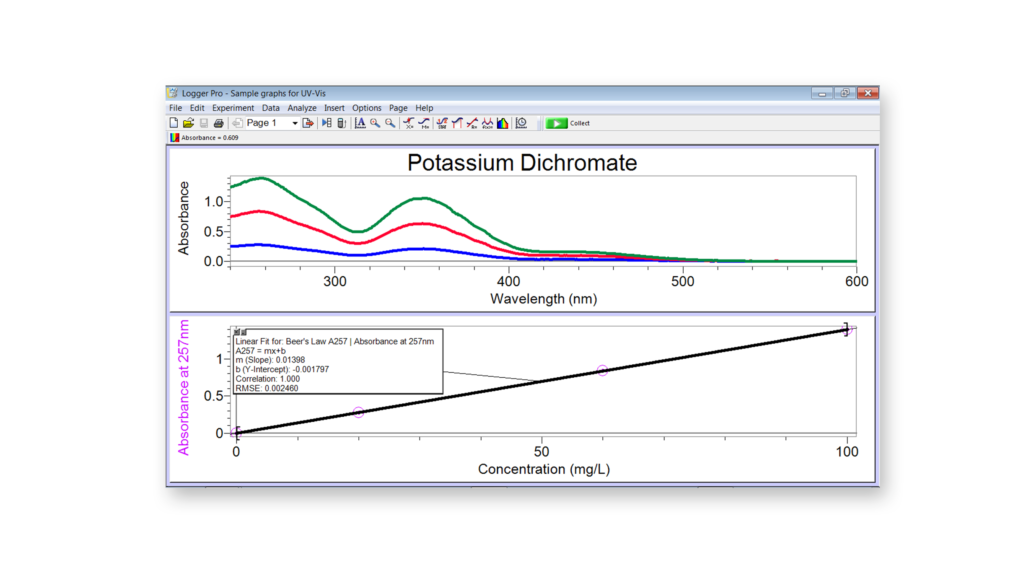
使用游标紫外-可见分光光度计和Logger Pro检查重铬酸钾的吸收光谱®
这只是可能的开始。请参阅下面的建议,开始学习分析化学。
免费实验下载
分析化学特色实验
酸碱滴定法
滴定是一种用于确定与给定量的另一种物质反应所需的溶液体积的过程。在这个实验中,你将用碱性氢氧化钠溶液NaOH滴定盐酸溶液HCl。NaOH溶液的浓度已经给出,你将确定未知的HCl浓度。在整个反应中,HCl中的氢离子与NaOH中的氢氧根离子以一对一的比例反应生成水:
当盐酸溶液与氢氧化钠溶液滴定时,酸性溶液的pH值最初很低。随着碱的加入,pH值的变化是相当缓慢的,直到接近等当点,当等摩尔量的酸和碱已经混合。在等当点附近,pH值迅速增加。pH值的变化再次变得更加缓慢,然后随着过量碱的加入而趋于平稳。
在这个实验中,你将在滴定时使用计算机监测pH值。pH值变化最快的区域将被用来确定等当点。等当点处NaOH滴定剂的体积将用于测定盐酸的摩尔浓度。
测定溶液浓度:比尔定律
本实验的主要目的是测定一种未知的硫酸镍溶液的浓度。要做到这一点,你将使用色度计或光谱仪让光穿过溶液,击中对面的探测器。所使用的光的波长应该是被溶液吸收的波长。的你4本实验中使用的溶液具有深绿色,因此色度计用户将被指示使用红色LED。光谱仪用户将根据溶液的吸收光谱确定适当的波长。撞击探测器的光被报告为吸光度或透光率百分比。高浓度的有色溶液比低浓度的溶液吸收更多的光(透射更少)。
你要配制五种已知浓度的硫酸镍溶液(标准溶液)。每一个都被转移到一个小的矩形比色皿中,再放入色度计或分光计中。穿透溶液并撞击探测器的光量被用来计算每种溶液的吸光度。当一个吸光度图vs。将标准溶液的浓度绘制成直线关系。溶液的吸光度和浓度之间的直接关系被称为比尔定律。
a的浓度未知的你4然后通过测量溶液的吸光度来确定溶液。通过在图的纵轴上定位未知物质的吸光度,可以在横轴上找到相应的浓度。未知物质的浓度也可以用比尔定律曲线的斜率求出来。
分析化学特色产品Manbetxapp手机
-
Go Direct®可见分光光度计
$1899 .00 -
Go Direct®UV-VIS分光光度计
$2499 .00 -
直接®荧光、紫外可见分光光度计
$2999 .00 -
直接®宽量程压力传感器
$199.00 -
游标式闪光光解光谱仪
$5799 .00 -
直接®铂电池电导率探针
$180.00 -
-
直接®宽范围温度探头
$128.00 -
直接®循环伏安法系统
$949.00 -